——2015年铜陵一中高三四、五月化学卷与高考安徽卷试题比较
一、三套试卷第25题的相似
2015年安徽高考:
25.(14分)
C、N、O、Al、Si、Cu是常见的六种元素。
(1)Si位于元素周期表第____周期第_____族。
(2)N的基态原子核外电子排布式为_____;Cu的基态原子最外层有___个电子。
(3)用“>”或“<”< span="">填空:
原子半径 | 电负性 | 熔点 | 沸点 |
Al_____Si | N____O | 金刚石_____晶体硅 | CH4____SiH4 |
(4)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。
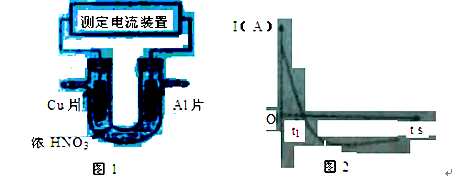
0-t1时,原电池的负极是Al片,此时,正极的电极反应式是_____,溶液中的H+向___极移动,t1时,原电池中电子流动方向发生改变,其原因是______。
四月卷: 25.(15分)原子序数依次增大的前四周期元素A、B、C、D、E、F、G,已知A是宇宙中含量最多的元素,D是地壳中含量最多的元素,B是形成化合物最多的元素,G是人类发现和使用最早的金属,我国历史上出现过火法冶炼和湿法冶炼。 E和F在同一周期,离子化合物EF,它是生活中常用的调味剂和防腐剂。根据以上信息,试回答下列问题(用元素符号等填写)
(1)G元素在周期表中的位置 ,其基态原子次外层有 个电子
(2)上述7种元素中,未成对电子数最多的元素,其基态原子电子排布式为
(3)A、E能形成离子化合物,该化合物溶于水,溶液呈碱性,该离子化合物电子式为
(4) C、D和稀有气体氖三种元素的第一电离能从大到小的顺序为 ; E、F形成的简单离子,离子半径从大到小的顺序为 (用离子符号填写)
(5)化合物GF(s)与O2反应生成,GF2(s)和一种黑色固体,在25℃,101KPa下,该反应每转移1mole-放热44.4kJ,该反应的热化学方程式为
五月卷:25.(14分)A、B、C、D、E五种短周期元素,其原子序数依次增大,A元素原子核外电子数等于其电子层数,B元素的基态原子核外3个能级上有电子,且每个能级上电子数相等,C元素原子最外层电子数为D元素原子最外层电子数的3倍,E元素的电负性是该周期中最大的。
(1)写出E元素基态原子核外电子排布式
(2)A、B、C、D四种元素的原子半径从大到小的顺序是 (用元素符号表示)
(3)D和E形成一种常见的离子化合物,用电子式表示其形成过程
(4)A、B、C三种元素形成一种有18个电子的分子,该分子的分子式是__________,该分子组成的物质沸点较高的主要原因是____________________________________ ______
(5)B和C能形成多种化合物,其中B3C2是一种在常温下有恶臭的气体,其分子中每个原子都满足最外层8电子结构,则B3C2的结构式是_____,分子的空间构型是______型
(6)已知B(s)+C2(g)=BC2(g) △H1=-akJ/mol,2D(s)+C2(g)=2DC(s) △H2=-bkJ/mol,
则1 mol D在BC2中完全燃烧放出热量 kJ。
★相似点分析:(1)考查的是元素在周期表中位置
(2)均考查了铜的核外电子排布的情况,我们的老师们在平时复习中也反复强 调,要求同学们掌握前四周期元素原子核外电子排布。
(3)五月卷对于热化学方程式也有考查
二、五月卷第28题与2015高考第12题、28题相似
五月卷:28.2014年冬天某校化学课外学习小组在实验探究中发现将镁粉投入到氯化铵溶液中,两者立即发生反应,产生了大量的气泡,经检验其中含有两种气体,一种气体有刺激性气味,请你根据所学的知识分析生成的气体可能为 和 (填化学式);
(1)①请你设计简单的实验方法检验上述实验中有刺激性气味的气体:
②实验开始时用校准过后的pH传感器测定纯水的pH,发现纯水的pH总是约在7.30左右,请分析其原因可能是 ;
③探究实验中0.2mol/L的氯化铵溶液pH为5.90,请用离子方程式表明该数据的原因
2015年高考12.某同学将光亮的镁条放入盛有NH4Cl溶液的试管中,有大量气泡产生。为探究该反应原理,该同学做了以下试验并观察到相关现象,由此得出的结论不合理的是:

★相似点分析:五月卷28题考查内容与高考完全相同,几个选项均有考查。铜陵一中的老师严格地按照考纲和考试说明的要求,研究高考内容,把握考试动态,注重重难点。
三、五月卷与2015年高考题26题相似
2015年高考题
26.(15分)
四苯基乙烯(TFE)及其衍生物具有诱导发光特性,在光电材料等领域应用前景广泛。以下是TFE的两条合成路线(部分试剂及反应条件省略):
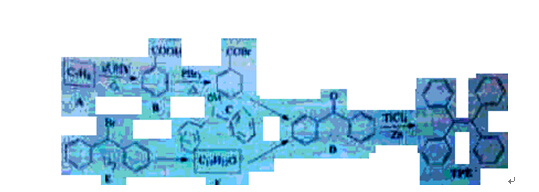
(1)A的名称是______;试剂Y为_____。
(2)B→C的反应类型为_______;B中官能团的名称是______,D中官能团的名称是______.。
(3)E→F的化学方程式是_______________________。
(4)W是D的同分异构体,具有下列结构特征:①属于萘(![]() )的一元取代物;②存在羟甲基(-CH2OH)。写出W所有可能的结构简式:_____。
)的一元取代物;②存在羟甲基(-CH2OH)。写出W所有可能的结构简式:_____。
(5)下列叙述正确的是______。
a.B的酸性比苯酚强 b.D不能发生还原反应
c.E含有3种不同化学环境的氢 d.TPE既属于芳香烃也属于烯烃
五月卷
26.(15分)已知:
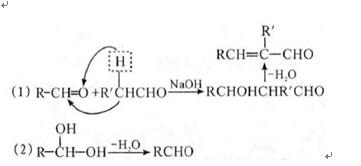
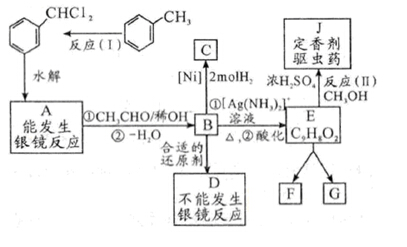 甲苯及其卤代物是有机化工的基本原料,由它出发可制造某些香料、药物及广泛应用于印刷,它们之间的关系如图所示。
甲苯及其卤代物是有机化工的基本原料,由它出发可制造某些香料、药物及广泛应用于印刷,它们之间的关系如图所示。
B、D、E都能使溴水褪色,E(分子式为C9H8O2)在光等辐射能作用下可以发生二聚加成反应,生成互为同分异构体的环状化合物F和G。请回答下面问题:
(1)写出有机物的结构简式:A ,C
(2)反应(I)的类型是 ,反应(Ⅱ) 类型是
(3)完成化学方程式:A→B 。
(4)同种类、互为同分异构体的F和G的结构简式为:F ,G
(5)对于上述各物质的转化关系中,下列说法正确的是
A.有机物D中含有的官能团是:羟基、碳碳双键和苯基
B.有机物J能在氢氧化钠中水解完全
C.有机物C可与金属钠反应,而有机物D不与金属钠反应
D.有机物E核磁共振氢谱为六组峰,且峰的面积比为2:2:1:1:1:1
★相似点分析:可以看出两道有机题都是从相同的原料----甲苯出发,考查了相同的反应类型,相同官能团名称,考查了卤代烃的水解,等效氢等知识点。相似度极高。
这些相似的题目不是巧合,而是命题组老师们辛苦钻研的成果。四月卷、五月卷都是我校化学命题组老师们经过了出题,审题,做题,查题这一系列劳动的成果,是老师们智慧的结晶,在高考最后一阶段为学生们的复习指明了方向